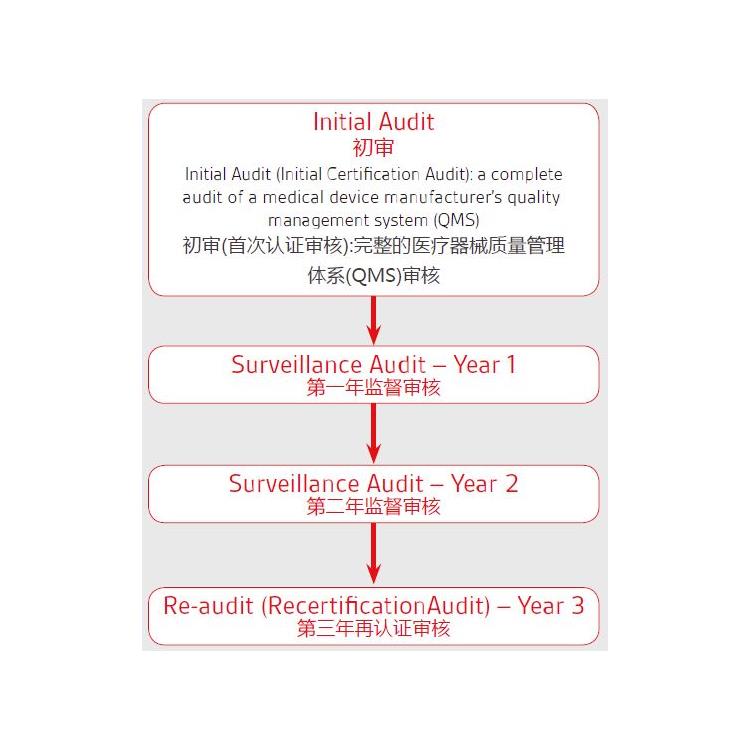
办理UK Responsible Person代理 办理英代生产厂家
价格:面议
产品规格:
产品数量:
包装说明:
关 键 词:办理英代生产厂家
行 业:咨询 管理咨询
发布时间:2022-12-14
英国脱欧后,按照脱欧协议,将陆续不再认可欧盟CE认证,对于器械,CE认证在英国可继续使用至2023年6月30日,但需要持有CE认证的企业在英国当地有英国负责人(类似欧盟授权代表),由英国负责人进行MHRA注册,才能进入英国GB地区市场(英格兰,威尔士和苏格兰)。2023年7月1日起,不再认可CE认证,必须进行UKCA认证。
什么是MDD/IVD
I类的器械MDD或者IVD other的产品
2021年12月31日起,需要做英国的DOC,然后贴加UKCA标志 以及确定英国代表,完成MHRA注册,然后才可以出口英国
需要办理以下认证可以随时找我 :
1:出口欧盟:MDR CE认证/IVDRCE认证,欧盟授权代表,欧盟注册,欧盟自由销售证书
2:出口英国:英国代表,英国MHRA注册,UKCA认证,英国自由销售证书
3:出口美国:美国FDA注册,FDA510K,QSR820体系
4:中国:国内的器械注册证和生产许可证
5:出口加拿大:加拿大的MDEL注册
6:质量管理体系认证:ISO13485咨询和认证
英国的法规是:英国法律(UK MDR 2002)(相当于欧盟的MDD/IVDD指令)
需要办理以下认证可以随时找我 :
1:出口欧盟:MDR CE认证/IVDRCE认证,欧盟授权代表,欧盟注册,欧盟自由销售证书
2:出口英国:英国代表,英国MHRA注册,UKCA认证,英国自由销售证书
3:出口美国:美国FDA注册,FDA510K,QSR820体系
4:中国:国内的器械注册证和生产许可证
5:出口加拿大:加拿大的MDEL注册
6:质量管理体系认证:ISO13485咨询和认证
欧盟授权代表是您与欧洲当局的联系的桥梁,他们必须是在欧洲有实体存在。
欧盟授权代表保存制造商的技术文件,供主管部门检查。
欧盟授权代表的名称和地址必须器械随附的信息上,例如(包装)标签和使用说明。如果发生事故,欧盟授权代表将协助并协调向主管当局报告事件。
MDR下的欧代相比于MDD下的欧代,要求更加严格,责任也更大。除了负有以上义务之外,还会与制造商一样为缺陷器械承担连带的法律责任。另外,授权代表应至少有一名可且持续听其调遣的负责法规符合性的人员,其在欧盟境内的器械要求方面拥有必要的知识。必要的知识应表现为以下任一一种:
(a) 在完成有关成员国确认为同等学历的法律、、、工程或其他相关科学学科大学学历或学习课程后颁发的文凭、证书或其他正式书,以及在体外器械相关法规事务或质量管理体系方面具有至少一年经验;
(b) 在法规事务或与器械有关的质量管理体系方面有四年的经验。
选择SUNGO,不是选择了一次性的合作伙伴,而是选择了一个长期的技术支持的战略伙伴。我们将秉承一贯“服务、客户”的原则,依托的技术团队,优化我们的服务,让更多的器械合法、进入市场,为器械行业健康发展贡献力量。