产品规格:
产品数量:
包装说明:
关 键 词:九江拭子的MDRCE认证
行 业:商务服务 认证服务
发布时间:2022-12-07
级医用防护服、隔离衣、手术衣,公告机构对产品技术文件进行预审;
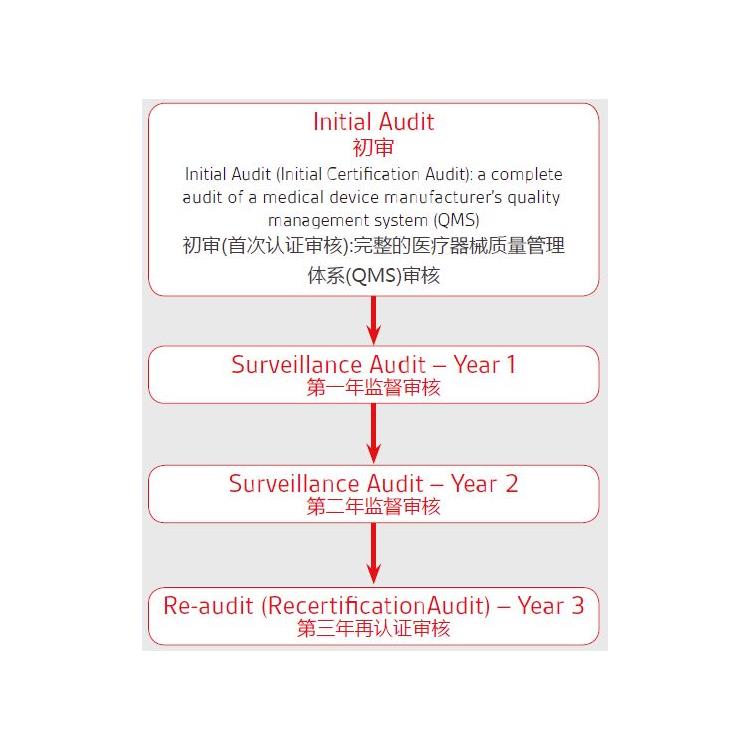
法规条款增加,认证评审更加严格
a. 分类规则增加:由MDD的18条增加到 22条;
b. 基本要求检查表条目增加:由MDD的13条增加到 MDR的23条;
c. CE技术文件的结构发生了变化,分为:产品技术文件和上市后文件(MDD只要求产品技术文件);
d.评价报告。MDR要求企业提供第四版评估报告,相比于第三版,第四版要求更为严格;
5:MDR要求更高的透明度和可追溯性
a. 引入了器械标识UDI,增加产品的可追溯性;
b. 企业的相关信息都会被收集到欧洲器械数据库(EUDAMED);
c. 建立上市后监督(PMS)系统;
办理出口:美国FDA注册(含FDA510K申请)、 FDA QSR820验厂及整改、FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改、CE认证(CE整套技术文件编订、 CE第四版评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016、欧盟授权代表、欧盟自由销售证书、英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
关于Free sale certificate自由销售证书,器械办理自由销售证书有三种:
种:中国食品药品监督管理局出局的器械产品出口销售
(这种办理条件:企业必须是生产企业,有国内的产品注册证&备案证,生产企业许可证&备案证,齐全,企业直接联系局,递交资料可以申请,不需要费用)
第二种:也是需要有注册证和许可证,可以由品商会这些出局的自由销售证书
(这种一般泰国,越南这些,也认可商会这种自由销售证书)
周期是一个半月左右
第三种:对于企业是否有中国的器械注册证和生产许可证,并没有特别的要求的。
我们市场常见 英国,德国 美国 荷兰等等这些发达出的自由销售证书的,这种尤其是被沙特,埃及,阿根廷等
这种主要看产品,如果在欧盟风险等级属于I类的话,不需要国内局的任何,配合填写申请表,说明书,符合性声明即可
如果在欧盟的风险等级属于II类的话,不需要国内局的任何,但是必须要有公告机构的CE证书才可以办理。
谁必须要申请FDA510(k)
FD&C Act的第510(k)规章中并没有特别指出谁必须申请510(k)——任何人都可以申请。但是,他们了哪种行为,例如把器械引入美国市场,要求510(k)申请。基于的行为,必须向FDA递交510(k)的有:
(1) 把器械引入美国市场的生产商;
(2) 把器械引入美国市场的研发设计者;
(3) 改变器械或器械标签的再包装者;
(4) 把器械引入美国市场的外国厂家/出口商或外国厂家/出口商的美国代理方
我公司办理:2022年已经获得30多个K号(产品主要有电动轮椅/手动轮椅/电动代步车/口罩/手术衣/隔离衣/手套等等)