产品规格:
产品数量:
包装说明:
关 键 词:纱布的MHRA注册厂家批发
行 业:商务服务 认证服务
发布时间:2022-12-01
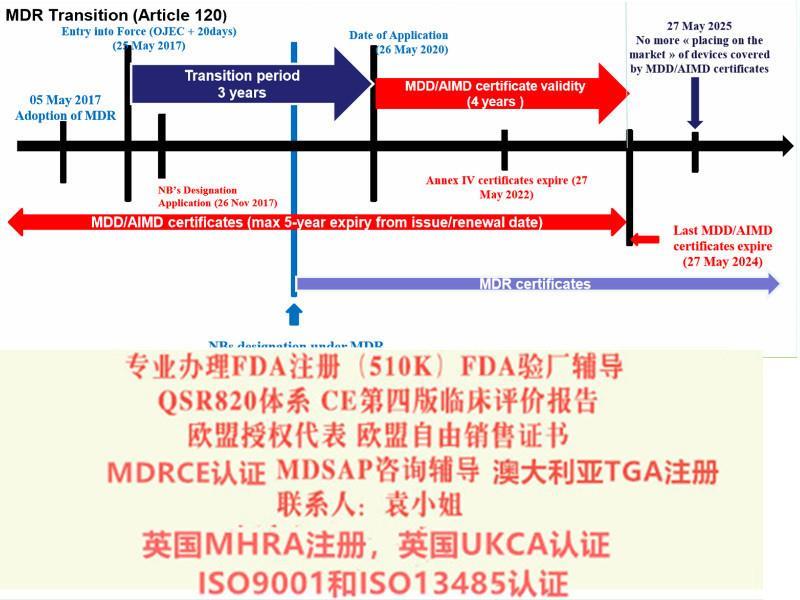
2017 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于器械第2017/七45 号法规(MDR,EU2017/七45),5月5日
我公司办理产品出口欧盟、美国、中东南美等的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
海牙成员国
尔巴尼亚、安道尔、安提瓜和巴布达、阿根廷、亚美尼亚、阿塞拜疆 澳大利亚、奥地利、巴哈马、巴巴多斯、白俄罗斯、比利时 伯利兹、波斯尼亚和黑塞哥维那、博茨瓦纳 文莱、保加利亚 香港和澳门 哥伦比亚、库克群岛、克罗地亚、塞浦路斯 捷克、丹麦、多米尼克,英联邦的、厄瓜多尔、萨尔瓦多、爱沙尼亚 斐济、芬兰、法国、格鲁吉亚(从2007年5月14日)德国 希腊 格林纳达 洪都拉斯、匈牙利、印度 冰岛、爱尔兰、以色列、意大利、日本 哈萨克斯坦 韩国、拉脱维亚、莱索托 利比里亚 列支敦士登、立陶宛、卢森堡、马其顿、马拉维、马耳他 马绍尔群岛、毛里求斯、墨西哥、摩尔多瓦(从2007年3月16日起) 摩纳哥、黑山、、荷兰、新西兰、纽埃 挪威、巴拿马、波兰、葡萄牙、罗马尼亚、俄罗斯联邦 圣基茨和尼维斯、圣卢西亚、圣文森特和格林纳丁斯、萨摩亚、圣马力诺 塞尔维亚、塞舌尔、斯洛伐克、斯洛文尼亚、南非、西班牙 苏里南、史瓦济兰、瑞典、瑞士、汤加、特里尼达和多巴哥 土耳其、乌克兰、英国、美国、委内瑞拉.
现在做出口认证的时候为什么会提到,甚至强调欧代?美代?
FDA注册时,都知道必须授权一个美国代理人,简称美代,可以是美国境内的普通人,也可以是一个企业,但是近年客户对于美代的要求越来越严格,美国境内的普通人远远无法解决企业遇到的问题,而且是经常的联系不上,美代没找好,没遇到问题还好,遇到问题了联系不上,严重的可能会让企业被开出警告信,产品出口受阻,选择一个好的美代很有必要。
欧盟授权代表,在CE认证时很多客户会选择的一项服务,虽然对于那些产品在欧盟法规上属于一类的产品法规规定是不需要加贴欧代信息的,但是现在欧盟对于I以上的 产品是必须加印欧代信息,而很多一类的产品客户也会选择欧代,同等于美代,欧代的重要性也显而易见。
欧代、美代主要是做什么的呢?
欧代、美代是企业与国外客户联系的纽带,国内外时间差异,产品一旦遇到问题,联系国内需要时间,这个时候可以联系美代,欧代了,当国外客户不能及时联系国内时,欧代、美代可以帮忙传达,所以,在认证时一定要选择比较有资质,比较好的企业作为自己的欧代。美代,避免关键时间联系不上
欧盟授权代表定义
欧盟授权代表(European Authorized Representative)是指由位于欧洲经济区EEA(包括EU与EFTA)的制造商明确的一个自然人或法人。该自然人或法人可代表EEA的制造商履行欧盟相关的指令和法律对该制造商所要求的特定的职责。
1)提供欧盟授权代表服务的公司是:SUNGO SUNGO Europe B.V. 该公司位于荷兰,为客户提供欧洲法规技术服务。凭借其能力,已经得到了荷兰局的认可提供相关技术服务,同时也被DNV, TUV等国际认证机构认可。目前已经为数百家客户提供了欧盟授权代表服务,为数百家客户提供了欧盟注册服务,同时还为一些客户提供了欧盟自由销售服务。
2)欧盟代表服务内容包括作为企业的联络人,负责处理欧盟市场上所有的客户投诉,、注册等业务。
3)五年有效期内一次清,无年度监督费用。
SUNGO可以在过渡期内为提供新旧法规的咨询服务,包括:
协助判定产品分类
协助选择合理的符合性途径
协助选择合适的认证机构
制定认证的解决方案
协助完成评估
编写CE技术文件
欧盟代表服务
欧代职责:
1. 代表欧盟非制造商与欧盟主管当局打交道
2. 欧盟代表保存新的,贴上CE标志产品的技术文件,确保随时及时的提供给欧盟主管当局审查。
3. 根据非欧盟制造商建立的警戒系统程序,欧盟授权代表协助其进行产品事故报告,召回等
4. 能为客户在欧盟境内销售产品时出现任何问题给予及时的信息沟通与协助解决。
5. SUNGO SUNGO Europe B.V. 总部位于荷兰,提供技术服务。主要业务是根据欧洲立法和国际标准,为客户提供完整的技术解决方案。SUNGO集团凭借全球网络和队伍为全球客户提供法规,在器械行业尤为专长。提供欧盟授权代表服务,可以为客户减少中间环节,节约时间和费用,使您的产品在符合现行欧盟法规的情况下进入市场的程序简单化。
6. SUNGO SUNGO Europe B.V.作为欧盟代表是被荷兰局局认可的。可以帮企业到欧盟主管注册,以免进入海关时出问题和引起法律纠纷,造成不必要的经济损失。
7. 欧盟出具的自由销售,目前针对器械做的比较多的是欧盟成员国的局出具的自由销售。SUNGO SUNGO Europe B.V. 可以办理。
我公司办理产品出口欧盟、美国、中东南美等的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
MDR分类规则的主要变化
分类规则: 5-8 Invasive devices
Rule 8:
• 在原来基础上,明确有源植入器械或其附件属于III类; 新增假体属于III类;关
节的全部或部分置换物(除钉、楔、板和工具等组件外)属于III类;除钉、楔、
板和工具等组件外的植入性椎间盘置换物和接触脊柱的植入器械属于III类。
这部分的修订取代了现有的指令:
• 90/385/EEC Active implant medical device
• 2003/12/EC Breast implants raised to Class III
• 2005/50/EC Hip, knee and shoulder joint replacements raised to Class III
分类规则: 9-12 Active devices
Rule 9:
• 在原来基础上, 增加对发射电离达到目的的有源器械,以及控制、这些器械或直接影响这些器械性能的有源器械属于IIb类;
• 在原来基础上, 增加预期用于控制、监视或直接影响有源植入器械性能的有源器械属于III类。
新增Rule 11:关于软件的分类规定,可以分为I, IIa, IIb,
III类:
• 提供用于作出诊断或目的决策的信息的软件,属于IIa类,除非这些决定有可能影响:
- 或个人健康状况不可逆转的恶化,属于III类;
- 个人的健康状况或手术严重恶化,属于IIb类。
• 用于监测生理过程属于IIa类,除非用于监测重要的生理参数,其中这些参数的变化可能导致对患者的即时危险,在这种情况下的软件属于IIb类。
• 其它属于I类
分类规则: 13-22 Special rules
Rule 16:
• 在原来基础上, 新增用于的器械属于IIa类,除非它们是用于侵入性器械的液或清洗机,这种器械属于IIb类。
分类规则: 13-22 Special rules
Rule 18:
• 在原来基础上, 增加由人体的组织或细胞,或其无活性或使其无活性的物合成或制成的器械属于III类。
分类规则: 13-22 Special rules
新增Rule 19:由纳米材料合成或制成的器械的分类规则。
• All devices incorporating or consisting of nano material are classified as:
– class III if they present a high or medium potential for internal exposure;
– class IIb if they present a low potential for internal exposure; and
– class IIa if they present a negligible potential for internal exposure
分类规则: 13-22 Special rules
新增Rule 20:
• 除侵入性器械外,其他通过人体孔道吸入方式来用药的侵入性器械属于IIa类,除非它们的作用方式对用药的性和有效性有至关重要的影响或用于危及生命的病症,在这种情况下属于IIb类。
我公司办理产品出口欧盟、美国、中东南美等的各种认证:
TUV莱茵,TUV南德等CE认证(MDD/MDR法规),CE技术文件编订, CE第四版评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改,英国BRC认证咨询,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令)。
我公司办理欧盟,美国,澳大利亚以及中东南美等等各类认证:FDA510K认证,欧盟自由销售证书,欧盟授权代表,ISO13485/ISO9001认证,欧盟CE认证(MDR(REGULATION (EU) 2019/745)),FDA注册,FDA验厂,英国授权代表,MHRA注册,美国代理人服务,澳大利亚TGA认证,CE整套技术文件编订、 CE第四版评价(MEDDEV 2.7.1 Rev 4)编写)、防护服PPE指令Type5/6认证、器械单一体系审核MDSAP认证、BSCI验厂、BRC 认证,澳大利亚TGA注册、口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试,器械产品备案登记表、器械产品注册证、生产备案登记表、生产许可证 MHRA器械注册(欧盟注册) 所有体外诊断器械(包括试剂)(IVD)和一类器械(Class I MD)在加贴CE标志(CE Marking)之前必须通过欧盟授权代表向其所在国的欧盟主管机构CA进行注册并取得注册证书和注册号码,否则将是违法的。 我公司可以作为欧盟授权代表,被英国MHRA批准可以代表企业向其申请注册证。注册企业信息可在线在MHRA查询 CFS 自由销售证 在国际贸易中,很多和地区需要制造商企业提供自由销售证。 自由销售证可以是制造商企业所在国的主管当局(例如中国局)签发的,也可以是第三国主管当局(例如英国局)签发的。 我公司可以为中国制造商企业申请CFS证书,不论是I类还是更高风险(需要取得CE证书)的产品。 办理Free Sale Certificate的流程是什么? 自由销售证书定义 自由销售证书也叫出口销售书,其英文名称为Free Sales Certificate、Certificate of Free Sale或者Certificate For Exportation of Medical Products;简称FSC 或 CFS。欧盟自由销售指的是欧盟的主管当局出具的产品可以在特定区域自由销售的文件。 谁可以获得CFS ? 目前欧洲所有的CFS只给位于其境内的公司颁发,这些公司可以是: 1、制造商; 2、欧盟代表; 3、贴牌厂商。 因此中国的制造商要申请CFS证书,只能是通过其欧盟授权代表来完成。 中国制造商申请CFS的条件 1、 了欧盟授权代表,签署了书面协议; 2、 产品有合法性的,这包括: 2. 1、 如果是I类的器械,提供DOC; 2. 2、 如果是I* IIA IIB III类器械,提供公告机构证书。
我公司办理:2022年已经获得30多个K号(产品主要有电动轮椅/手动轮椅/电动代步车/口罩/手术衣/隔离衣/手套等等)