北京医疗器械单一体系审核MDSAP认证是什么 欢迎咨询
价格:面议
对MDSAP审核结果的认可,绝不意味着主管当局放弃其监管权力。
日本MDSAP:对于II类,III类,IV类器械,可豁免现场工厂审核;
医疗器械单一体系审核MDSAP认证咨询辅导
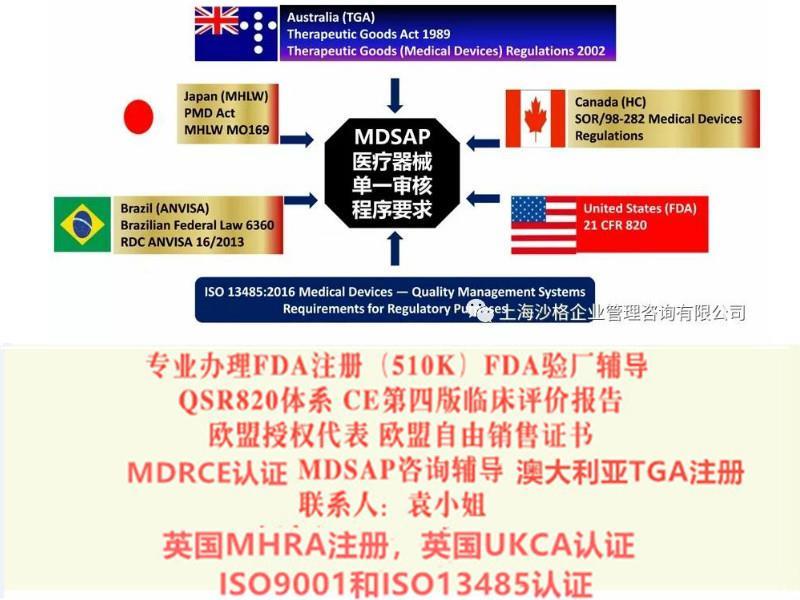
美国,澳大利亚,巴西,加拿大,日本五国的监管机构,加入“医疗器械单一审核程序(Medical Device Single Audit Program (MDSA))”项目并试行。该程序旨在建立一套单一审核的过程,满足并统一上述国家的审核要求,使审核更加全面有效。
2015年1月1日,在全球范围内,对于美国,澳大利亚,巴西,加拿大市场感兴趣的生产企业受邀参加了该项目。去年夏天,日本正式成为MDSAP的一员,对于日本市场感兴趣的生产企业也将受到该项邀请。
MDSAP由第三方进行审核,参与国的医疗器械监管部门可以将此审核报告作为判断依据。MDSAP不仅减少了监管部门例行检查的工作,也使得各监督部门共享相同且可靠的审核结果。
由于监管机构认可MDSAP的审核结果,生产企业可以减少对应不同监管机构的审核次数,减少因审核带来的生产干扰。MDSAP的出台,使审核过程国际标准化,减轻了生产企业的负担。MDSAP的审核依照参与国的已有法规要求,不额外增加其他要求,绝大多数情况下,各国的要求采用的是协调标准或标准内容基本类似,例如:医疗器械质量管理体系用于法规的要求(ISO 13485:二016),巴西的良好生产规范(RDC ANVISA 16/二013),美国质量体系规范 (21 CFR Part 820)和MDSAP参与国的其他特定上市前和上市后的法规要求。
美国FDA
接受MDSAP的审核代替FDA的例行检查,每两年对所有类别的医疗器械,包括体外诊断设备进行MDSAP审核,但上市前审核(PMA)和投诉检查不能用MDSAP替代。
通过生产企业的不断参与,MDSAP项目将会逐渐完善,预计将于2019年正式运行。MDSAP将会提升第三方机构的公信力,推动各国法规及审核标准的统一,扩展针对患者保护的全球安全网络。
MDSAP 的优势
通过MDSAP审核将:
? 减轻医疗器械制造企业多重法规审核的负担
? 提供可预测的审核计划(包括审核开始和结束日程)
? 利于患者的健康和了解(消除工厂审核的障碍)
? 优化监管资源配置
? 可与ISO 13485和CE符合性审核相结合
? 多国法规要求一次审核完成
-/gjhdff/-