TUV莱茵的MDR-CE认证 mdr检测是什么意思 的流程及步骤
价格:面议
产品规格:
产品数量:
包装说明:
关 键 词:TUV莱茵的MDR-CE认证
行 业:商务服务 认证服务
发布时间:2023-09-08
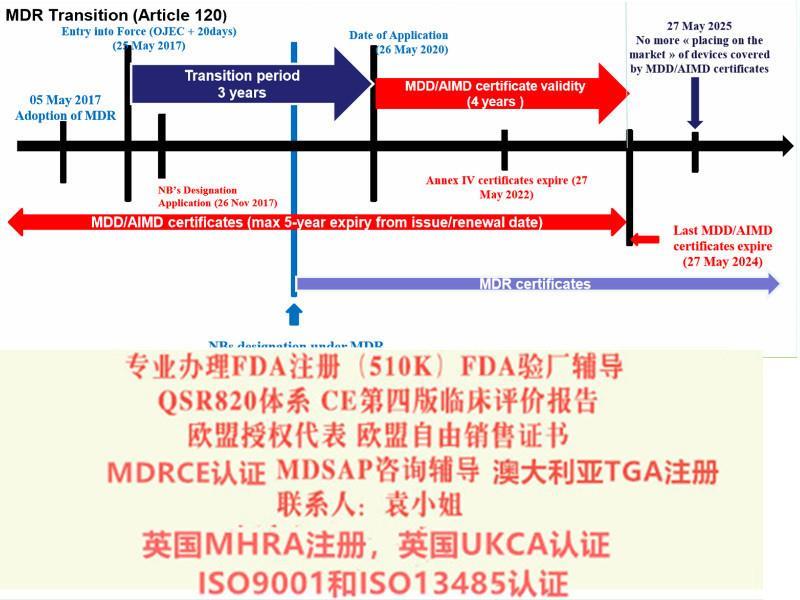
关于欧盟CE 认证的MDR 2017/745法规升级,关于的过渡期:
仅拥有根据指令90/385/EEC和93/42/EEC颁发的的设备可以投放市场,前提是自MDR应用之日起设计和预期用途没有发生重大变化且符合要求新规定。,市场监督,警报,经济运营和设备登记的规定。
中国工厂在注册过程中,需要工厂配合提供相关资料,大概的资料清单如下(具体要以实际客户提供的为准):
1 . Exclusive distribution certificate original ( Attested from Embassy of and Legalised From local magistrate )
2. CE Certificate
3. Declaration of conformity original ( Attested from embassy of and legalised from local magistrate )
4. 13485 CE certificate
5. Manufacturing Process details documentation
6. credentials of the company duly attested original seal
7. essential principle of safety
8. Free sale certificate from Europe customer ( Duly attested from Embassy of )
2017年5月5日,欧盟(Official Journal of the European Union)正式发布了欧盟器械法规(REGULATION (EU) 2017/745,简称“MDR”)。
产品名称和商品名、产品代码、目录编号或欧盟符合性声明中包含的其他允许识别和追溯产品的明确的参考号,如适当照片,以及适当时其预期目的。除产品或商品名称外,第3条中基本UDI – DI所提供的允许识别和可追溯产品的信息
按照附录VIII的规则所划分的器械风险等级
当前声明所涵盖的器械符合本法规,以及适用时其他相关的要求签署欧盟符合性声明的欧盟立法的声明
出口英国需要办理UKCA认证:随着2020 年12 月31 日英国脱欧过渡期结束,2021 年1 月1 日期英国企业器械产品在英国上市,要求符合UKCA 要求。
手术衣510K,隔离衣510K,手套510K,电动/手动轮椅510K,FDA注册,FDA美国代理人