产品规格:
产品数量:
包装说明:
关 键 词:淮安拭子的MDRCE认证
行 业:商务服务 认证服务
发布时间:2023-02-18
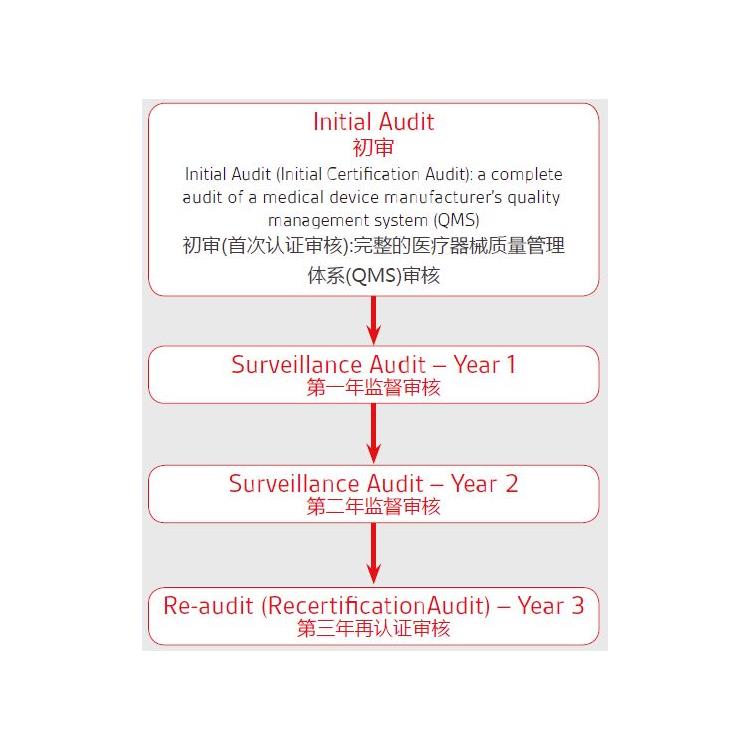
关于欧盟CE 认证的MDR 2017/745法规升级:
老指令MDD 93/42/EEC including 2007/47/EC 升级到新法规MDR EU 2017/745
2017年5月,欧盟器械新法规MDR (REGULATION EU 2017/745) 颁布,新的法规将替代原有的器械指令 (MDD 93/42/EEC) 和有源植入性器械指令 (AIMDD 90/385/EEC) 。
对于变更事项的规定,欧盟法规更接近产品本身,如涉及设计或特性的更改、协调标准更改等,使得变更事项更为明确。另外,欧盟在符合性评估过程中允许产品发生变化,相比于中国法规审评审批过程中无法变更的要求,这种方式更为灵活;充分利用UDI 及电子数据系统等工具, 从欧盟法规层面规定了电子系统的建立和使用要求,从而增加器械上市的透明度和可追溯性。
主要变化之九:风险-收益
附件7提供了详细的指南,对于器械的性和性能表述;
附件7.2 讨论了风险和收益分析,包括对于风险和收益的量的评估,以及总体评价。交付后的数据价值,以及可能会影响统计有效性行的因素等。
如何选择EAR
EAR并非特定授予的资质或认可,没有第三方评价资质可以参考。任何一个能够履行欧盟法规特定职责的欧盟成员国境内自然人或法人都能够成为EAR。但EAR不仅仅是提供了一个欧洲境内的注册地和响应代表,合格的EAR还应当:
1)具有的法规和法律能力,帮助企业咨询、了解并响应欧盟法规;
2)合法的帮助制造商在欧盟境内注册相应设备和器械;
3)有充足的技术能力验证并评审企业技术文件,实施内部评审,降低质量风险;
4)具有一个良好的公共关系纽带,有丰富的经验帮助制造商与欧盟有关部门沟通并解决问题;
5)跟进法规更新,了解熟悉MDR,清晰识别EAR职责,有能力确保制造商符合要求。
[img/new19/sungo99/1596099175.jpg[/img]
出于节约成本的考虑,制造商自己的进口商或贸易律师等都可以是EAR的选择之一。为了更好地符合欧盟要求以及减少风险,也可选择的EAR代理机构。充分考察EAR的沟通能力、响应时效、信息准确性、规模和、行业口碑等,是选择合格EAR的重要依据。
依据MDR Article 123的要求,MDR于2017年5月26日正式生效,并与2020年5月26日期正式取代MDD(93/42/EEC)和AIMDD(90/385/EEC)。日前公告机构BSI获得了欧盟新法规MDR(EU 2017/745)的授权。也意味着近期BSI、TUV南德、TUV莱茵、SGS等公告机构,也陆续可以开始受理MDR的申请。MDR实施之后,在三年过渡期内仍然可以按照MDD和AIMDD申请CE证并保持证的有效性。依据Article 120 clause2 的规定,过渡期内NB签发的CE证继续有效,但是从其交付日期起有效期不超过5年,并且于2024年5月27日失效。
所有客户均有专属服务人员,针对市场准入过程中的问题提供的支持和解答。选择SUNGO,不是选择了一次性的合作伙伴,而是选择了一个长期的技术支持的战略伙伴。