棉签CE*四版临床评价报告 临床试验评价报告 申请条件
价格:0.00起
产品规格:
产品数量:
包装说明:
关 键 词:棉签CE*四版临床评价报告
行 业:商务服务 认证服务
发布时间:2023-08-24
对制造商和产品的影响而言,93/42 EEC指令和MDR基本上具有相同的基本要求。没有现有的需求,但是MDR添加了新的需求,与目前93/42指令相比,MDR更加强调生命周期方法的性,并有数据支持。MDR对公告机构的提出了更严格的要求,对主管当局和会加强了控制和监测。
需要办理以下认证可以随时找我 : 1:出口欧盟:MDR CE认证/IVDRCE认证,欧盟授权代表,欧盟注册,欧盟自由销售证书 2:出口英国:英国代表,英国MHRA注册,UKCA认证,英国自由销售证书 3:出口美国:美国FDA注册,FDA510K,QSR820体系 4:中国:国内的器械注册证和生产许可证 5:出口加拿大:加拿大的MDEL注册 6:质量管理体系认证:ISO13485咨询和认证

MDR的主要变化 1.扩大了应用范围 2.提出了新的概念和器械的定义 3.细化了器械的分类 4.完善了器械的通用和性能要求 5.加强对技术文件的要求 6.加强器械上市后的 7.完善评价相关要求 8.提出Eudamed数据库的建立和使用 9.提出器械的可追溯性(UDI) 10.对NB提出严格的要求
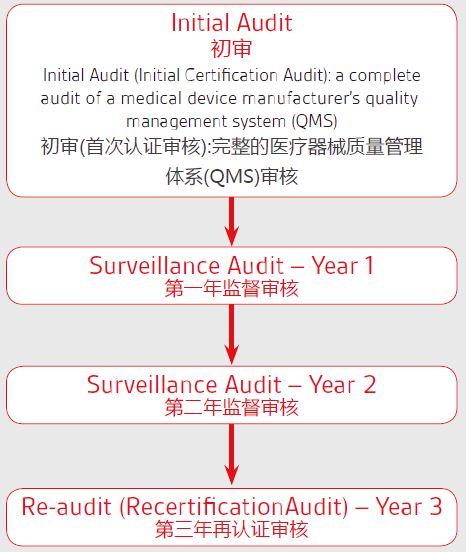
CE*四版评价报告MEDDEV 2.7.1 Rev4主要变化
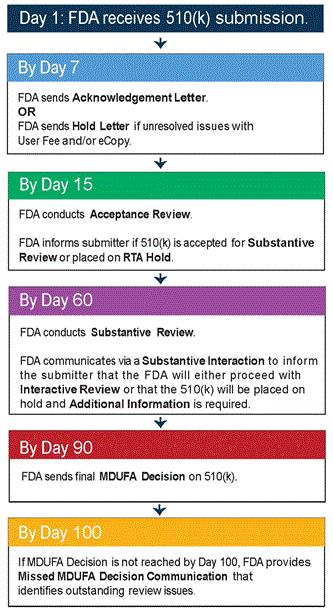
我公司是做: 1:新MDR法规和MDD指令的欧盟CE认证,CE*四版评价报告更新/编写 2:欧盟自由销售证书,欧盟授权代表(德国,荷兰,英国), 3:ISO9001/ISO13485认证以及咨询 4:FDA注册,FDA510K,FDA验厂/陪审和翻译 5:MDSAP咨询,国内注册证,生产许可证的办理
SUNGO服务的宗旨不仅是完成项目,而是帮助客户解决问题并达成目标。所有客户均有专属服务人员,针对市场准入过程中的问题提供的支持和解答。选择SUNGO,不是选择了一次性的合作伙伴,而是选择了一个长期的技术支持的战略伙伴。








