首页 > 供应商机 > 医疗器械生物学评价试验_无锡生物学检验中心
医疗器械生物学评价试验_无锡生物学检验中心
价格:1800起
威科检测集团有限公司
联系人:欧阳工
电话:13570966673
地址:广东省广州市东凌广场A座
产品规格:
产品数量:30 个
包装说明:
关 键 词:无锡生物学检验中心
行 业:环保 环境检测服务 生物检测
发布时间:2023-04-24
生物学评价检测选择和原则
无论国内还是国外,批准的都是以产品形式提供的医疗器械产品,而非用于制造医疗器械的各种材料。因此,生物学评价是对终成品的评价。医疗器械产品的生物相容性不仅取决于材料本身,还取决于材料的加工、生产方式(包括方法),以及可能存在于终产品中的加工残留物。
生物学评价报告:生物学测试和评估结果的生物学评价报告是医疗器械产品注册申报的重要技术文件,用于确定所获取的信息是否已充分满足生物学性评价的目的并得出产品是否性的结论,属于产品风险管理的一部分。
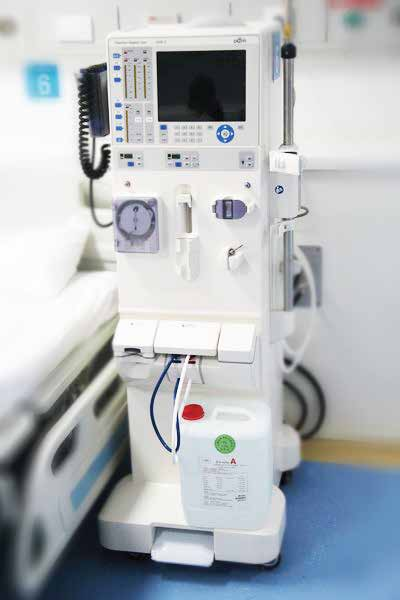
生物学评价试验包括细胞毒性、致敏、或皮内反应、全身毒性、遗传毒性、植入、血液相容性等测试项目,对于某种医疗器械产品,一般根据实际使用过程中与人体的接触性质(表面器械、外部接入器械、植入器械)和接触时间来选择试验项目,具体可参考表1。例如,表面器械压迫止血带产品,因其短时间与皮肤接触,可考虑进行细胞毒性、致敏以及或皮内反应测试;外接透析器产品,因长时间接触循环血液,还需考虑全身毒性、植入、血液相容性等测试。此外,对医疗器械所识别出的所有试验并非都是必须要进行或可行的,应根据每种器械的具体情况考虑应做的试验。
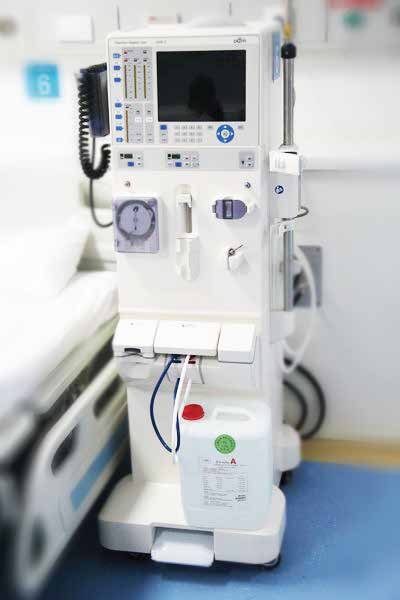
针对材料的生物相容性文献数据是否足以支持医疗器械的生物相容性,医疗器械所用材料已有的生物相容性的文献数据可能不足以支持由该材料制造的器械的生物相容性,其原因是制造和加工工艺可能会影响体内器械的终化学状态。
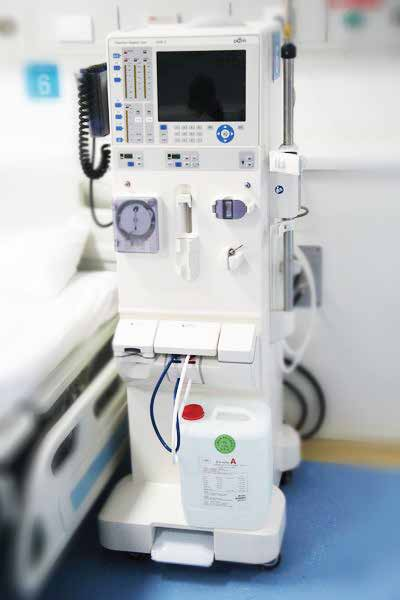
生物学评价标准分别是:GB/T16886医疗器械生物学评价,*1部分:评价与试验;*2部分:动物保护要求;*3部分:遗传毒性、致癌性和生殖毒性试验;*4部分:与血液相互作用试验选择;*5部分:体外细胞毒性试验;*6部分:植入后局部反应试验;*7部分:环氧乙烷残留量;*8部分:生物学试验参照样品的选择和定性指南;*9部分:潜在降解产物定性与定量框架;*10部分:与致敏试验;*11部分:全身毒性试验;*12部分:样品制备与参照样品;*13部分:聚合物医疗器械的降解产物定性与定量;*14部分:陶瓷降解产物定性与定量;*15部分:金属与合金降解产物定性与定量;*16部分:降解产物和可溶出物的毒代动力学研究设计;*17部分:可沥滤物允许**的确立;*18部分:材料化学表征;*19部分:材料物理化学、形态学和表面特性表征;*20部分:医疗器械*毒理学试验原则与方法;ISO/CD10993-21生物医学材料生物学评价标准编写指南。
原材料来源改变为何需要重新进行生物学评价?
答:聚合物供应商发生改变往往需要重新评价。例如,如果新的树脂供应商缺少加工溶剂的处理步骤(其中一些可能是已知的有毒化合物,如),跟利用原始树脂制造的器械相比,制造出的终器械可能产生未知毒性。








